SAS Life Science Analytics Framework: Rückenwind für klinische Studien und Medikamentenentwicklung

Heidelberg, 26. Juli 2022 – SAS unterstützt die Life-Science-Branche bei ihren größten Herausforderungen: die riesigen Datenmengen im Rahmen von klinischen Studien schnell zu verwertbaren Informationen zu machen und den äußerst komplexen Zulassungsprozess zu steuern. Der Experte für Analytics und künstliche Intelligenz (KI) stellt mit SAS Life Science Analytics Framework auf Azure eine leistungsstarke Cloud-Technologie für den Life-Science-Sektor bereit, die Machine Learning, KI und Analytics für das Internet of Things (IoT) nutzt.
Die Advanced-Analytics-Plattform, die als integrierte, offene, Cloud-native Computing-Umgebung für die Analyse und Einreichung von klinischen Studien (https://www.sas.com/de_de/solutions/cloud/microsoft-azure/solution/transforming-clinical-trial-analysis-submission.html)dient, hilft pharmazeutischen Unternehmen dabei, den stark regulierten Bereich der Analyse zu managen und so neue Therapieansätze schneller zur Anwendung zu bringen.
Analytics in der Cloud
Die klinische Forschung, die einer Zulassung durch die Behörden vorangehen muss, bringt sehr große Mengen an Daten mit sich – und damit hohe Anforderungen an die Verwaltung, Bereitstellung und Analyse dieser Daten.
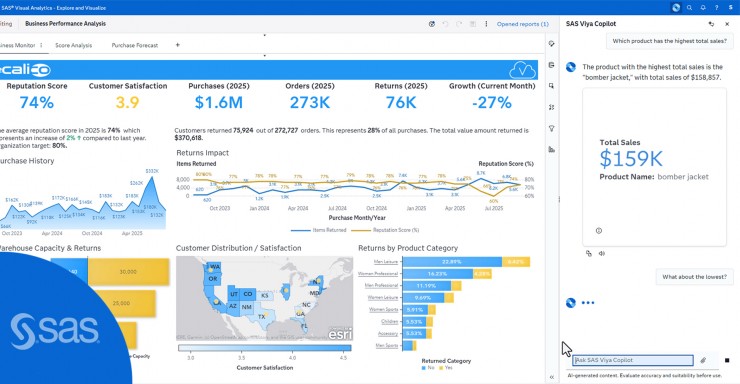
Das Cloud-basierte SAS Life Science Analytics Framework auf Azure stellt eine integrierte Kollaborationsumgebung bereit, mit der sich Informationen zu klinischen Studien managen und analysieren lassen; gleichzeitig können darüber Ergebnisse dieser Studien den Behörden zur Verfügung gestellt werden. Auf diese Weise bekommen Arzneimittelhersteller und Forschungseinrichtungen wertvolle Erkenntnisse aus klinischen Daten, können Risiken minimieren, die Effizienz erhöhen und die Time-to-Market für Medikamente beschleunigen.
Die in Washington ansässige US-Forschungseinrichtung Gunvatta (https://www.sas.com/de_de/customers/gunvatta.html) hat ihr Vorgehen bei klinischen Studien mit dem SAS Life Science Analytics Framework modernisiert. Sie hilft Pharmaunternehmen dabei, Risiken durch einen sicheren Zugang zu Daten zu minimieren, Informationen und Forschungsergebnisse zuverlässig zu validieren, den Auditierungsprozess einzuhalten und ihre Daten an die Behörden zu melden.
Spezialisierte Tools für die klinische Forschung
Mit der SAS Clinical Enrollment Simulation Cloud wird SAS eine Cloud-native Lösung auf SAS Viya (https://www.sas.com/de_de/software/viya.html) auf den Markt bringen, die es Unternehmen und Institutionen ermöglicht, das Ergebnis des komplexen Zulassungsprozesses bei klinischen Studien digital zu simulieren. Dadurch werden Hindernisse frühzeitig erkannt und Zulassungsprozesse erheblich beschleunigt.
Das SaaS-Angebot soll Ende des Jahres auf dem Microsoft Azure Marketplace verfügbar sein und nutzt eine separate leistungsstarke Analytics-Engine, um den Zulassungsprozess im Zeitverlauf zu modellieren. Dies ermöglicht eine durchgängige Kontrolle der Strategie, so dass eine schnelle Umsetzung neuer Ansätze in der Praxis ermöglicht.
“Die SAS Clinical Enrollment Simulation Cloud hebt sich deutlich von herkömmlichen Methoden ab, mit denen bisher die Zulassungsprozesse und -chancen für klinische Studien simuliert wurden”, erklärt Jim Box, Life Sciences Principal Data Scientist bei SAS. “Die Technologie verschafft Life-Science-Unternehmen zahlreiche Vorteile: kürzere Vorlaufzeiten, geringere Kosten und bessere Erkenntnisse, die zu einer fundierten Planung und einem sicheren Abschluss klinischer Studien führen.”
COVID als Katalysator für die Modernisierung klinischer Studien
Nicht zuletzt die Pandemie hat Bewegung in die Vorgehensweise bei klinischen Studien gebracht, die durch die bisher eingesetzten Forschungsmodelle oftmals verlangsamt wurden, womit sichere, kosteneffektive Therapien auf sich warten ließen.
“Die positiven Auswirkungen auf den Life-Science-Sektor liegen in der wesentlich schnelleren digitalen Transformation und der Modernisierung der Forschung”, sagt Simon Tilley, Health and Life Sciences Product Director bei SAS. “Der Boden war bereitet für innovative Ansätze wie dezentralisierte Studien zur Entwicklung neuer Impfstoffe. Von den schnelleren Prozessen zur Zulassung profitieren letztlich die Patienten unmittelbar.”
Weitere Informationen liefert das Whitepaper “Decentralized Clinical Trials: From Evolution to Revolution”.
circa 4.000 Zeichen
SAS Institute GmbH
Thomas Maier
In der Neckarhelle 162
69118 Heidelberg
Deutschland
E-Mail: thomas.maier@sas.com
Homepage: https://www.sas.com/de_de/home.html
Telefon: 0049 6221 415-1214
Pressekontakt
Dr. Haffa & Partner GmbH
Anja Klauck
Karlstraße 42
80333 München
Deutschland
E-Mail: postbox@haffapartner.de
Homepage: http://www.haffapartner.de
Telefon: 089 993191-0